| початок розділу
Виробничі, аматорські радіоаматорські Авіамодельний, ракетомодельного Корисні, цікаві |
хитрощі майстру
електроніка фізика технології винаходи |
таємниці космосу
таємниці Землі таємниці Океану хитрощі Карта розділу |
|
| Використання матеріалів сайту дозволяється за умови посилання (для сайтів - гіперпосилання) | |||
Навігація: => |
На головну / Каталог патентів / В розділ каталогу / Назад / |
|
ВИНАХІД
Патент Російської Федерації RU2241983
![]()
СПОСІБ ВИЗНАЧЕННЯ ренію І ренію В ПРИСУТНОСТІ МОЛІБДЕНУ МЕТОДОМ інверсійної вольтамперометрії
Ім'я винахідника: Колпакова Н.А. (RU); Гольц Л.Г. (RU); Августинович О.В.
Ім'я патентовласника: Томський політехнічний університет
Адреса для листування: 634034, Томськ, пр. Леніна, 30, Томський політехнічний університет
Дата початку дії патенту: 2003.11.11
Використання: в різних галузях народного господарства для визначення вмісту в розчинах концентрацій різних іонів металів. Сутність: спосіб визначення іонів металів включає визначення ренію і ренію в присутності молібдену на тлі 1 М HNO 3 з додаванням 0,1 г KNO 3 методом інверсійної вольтамперометрії (ІВА), при якому проводиться електроконцентрірованіе ренію на графітовому електроді з подальшим окисленням осаду. Технічним результатом винаходу є підвищення чутливості більш ніж на 2-3 порядки і зниження часу аналізу.
ОПИС ВИНАХОДИ
Винахід відноситься до аналітичної хімії, а саме до способів визначення іонів металів, і може бути використано в гідрометалургії, в різних геологічних розробках при пошуку і розвідці в разі аналізу руд, а й в нафтохімії для визначення вмісту в розчинах, рудах і рудних концентратах концентрацій іонів ренію методом інверсійної вольтамперометрії (ІВА).
Полярографическое поведінку ренію вивчено в розчинах кислот (НСl, НСlO 4, H 2 SO 4, Н 3 РO 4, НNО 3, оцтова кислота), в нейтральних розчинах хлоридів калію і натрію, а й лужних розчинів [Л.В. Борисова, А.Н. Єрмаков. Аналітична хімія ренію, - М: Видавництво "Наука", 1974, 315 с.].
Поведінка ренію в соляно і хлорнокіслий розчинах. Максимальна висота хвилі відновлення ренію спостерігається в 2-4,3 N НСl [Lingune JJJAm.Chem.Soc., 64, 1001, 2182 (1942); 65, 866 (1943)]. Потенціал напівхвилі E 1/2 для ренію (VII) в 2 М НСl дорівнює -0,45 В, а в 4,2 М НСl -0,31 В. Недоліком цього процесу є те, що визначення ренію заважають іони NO -3, SO 24, РO 34, які спотворюють лінію фону, а й молібден і вольфрам, які є супутніми елементами ренію в рудах і рудних концентратах.
Поведінка ренію в сірчано і фосфорнокислий розчинах. Гейер показав [Gеуеr RZ anorg. allgem. Chem., 263, 47 (1950)], що число хвиль відновлення і їх характер змінюється в залежності від концентрації H 2 SO 4. Потенціал напівхвилі E 1/2 для ренію (VII) в 3,5 М H 2 SO 4 дорівнює від 0,2 до -0,45 В. В цьому випадку визначення ренію заважають аніони Сl -, NO -, РO 34, а й Мо, Fe і Ti.
Поведінка ренію в нейтральних, лужних і буферних розчинах. Застосування полярографії в нейтральних і лужних розчинах найбільш доцільно для визначення невеликих концентрацій ренію [Рубинская Т.Я., Майрановський С.Г. Електрохімія, 7, 1403 (1971)]. Каталітичні хвилі, придатні для аналітичних цілей, відповідають від -1,2 до -1,6 В. В даному процесі заважає вплив надають іони Cl -, NO -3, SO 24, РO 34 і Мо, Сu, Zn , Cd, Pb, Bi, Se, Co і W.
Поведінка ренію в розчинах азотної кислоти. Осцилографічний метод дозволив спостерігати катодний хвилю відновлення ренію. У 1М НNО 3 потенціал напівхвилі для ренію дорівнює -0,6 В. Межі виявлення становили 10 -3 -10 -4%. Заважають елементами є Мо, Сu, Zn і W, а й аніони Сl - і ін.
Відомі полярографічні методи визначення ренію, які діляться на 2 групи:
а) методи визначення великих кількостей (від 10 -3% і вище), засновані на вимірі хвиль відновлення перрената;
б) методи визначення мікрокількостей ренію в інтервалі 10 -3 -10 -7%, що використовують каталітичні струми і концентрування ренію на електроді у вигляді малорастворимой плівки оксиду.
Зміст ренію в сплавах від 2 · 10 -1% і більше визначають зазвичай по хвилі з E 1/2 = (- 0,3) - (-0,4) В на тлі 2,5 М H 2 SO 4. Менші кількості ренію (до 10 -3%) в продуктах мідно-молібденового виробництва визначають по каталітичної хвилі водню з E 1/2 = -1,2 В на тлі фосфатного буферного розчину (рН 7-8). Недоліком методу є те, що молібден попередньо відокремлюють у вигляді труднорастворимого молибдата кальцію спеканием проби з СаО при 600-700 ° С протягом 2 год. Докладний хід аналізу наведено в [Крюкова Т.А., Синякова С.І., Ареф'єва Т. В. Полярографический аналіз. М., Госхіміздат, 1959, стор. 351].
Молібденові концентрати рекомендується розкладати і конц. НNО 3 з подальшою дистиляцією Re 2 O 7 з сірчанокислого розчину [Duca A., Stanescu D., Puscasu М. Studii si cercetari chim. Acad. RPRFil. Cluj, 6, 123 (1955); 13,197 (1962)]. Визначення ренію проводять на тлі розчину NaCl + Na 2 SO 3 (pH 11,3-11,5) при молярному співвідношенні Mo: Re ![]() 200: 1 і E 1/2 = -0,45 В. відкривається, мінімум дорівнює 1-2 мкг Re / мл. Визначення проводять і після пробопідготовки, в ході якої від ренію відокремлюються молібден, вольфрам та інші супутні елементи.
200: 1 і E 1/2 = -0,45 В. відкривається, мінімум дорівнює 1-2 мкг Re / мл. Визначення проводять і після пробопідготовки, в ході якої від ренію відокремлюються молібден, вольфрам та інші супутні елементи.
Чутливим методом є інверсійної-вольтамперометрических метод визначення ренію на тлі 4М Н 3 РO 4 із застосуванням осциллографического полярографа і ртутного стаціонарного мікроелектрода [Демкин А.М., Синякова С.І. Зб. "Визначення мікродомішок". М., ДНТП, 1968, стор. 31] (прототип). Визначення ренію проводять за такою методикою. Аліквотну частина 5-10 мл (4М Н 3 РO 4), що містить ~ 0,01-0,1 мкг Re, поміщають в електролітичну комірку. Протягом 3 хв через розчин продувають азот, встановлюють на Осциллографическое полярограф режим анодної поляризації і потенціал ртутного мікроелектрода, що дорівнює 0,95 В. Реєструють хвилю при цьому потенціал. Необхідною умовою процесу є те, що реній в пробах відділяється від молібдену і вольфраму. Ця умова є одним з недоліків цього методу.
Основним завданням запропонованого нами рішення є визначення ренію і ренію в присутності молібдену на импрегнірованого графитовом електроді методом ІВА.
Поставлена задача досягається тим, що реній хімічно концентрують на різних типах графітових електродів (стеклоуглеродном (СУ), ртутно-плівковому (РП) або импрегнірованого графитовом (ІГ)) з подальшою реєстрацією анодних вольтамперограмм. Новим у способі є те, що проводять накопичення ренію в перемішувати розчині протягом 120-150 с при потенціалах електролізу Е е = (- 0,7) - (- 1,0) В на тлі: 1 М HNO 3 c додаванням 0, 1 г КNO 3 з подальшою реєстрацією анодних піків в накопичувальному режимі зйомки вольтамперограмм при швидкості розгортки 30-50 мВ / с. Концентрацію ренію і ренію в присутності молібдену визначають по висоті анодного піка в діапазоні потенціалів від 0,150 до 0,250 В відносно насиченого хлорідсеребряного електрода (нас.х.е.).
У прототипі кількісне визначення ренію засноване на реакції відновлення і можливо тільки після ретельного відділення його від молібдену, який часто є супутнім елементом ренію в рудах і рудних концентратах.
У пропонованому способі вперше встановлена здатність ренію окислюватися на різних типах графітових електродів. Як індикаторних застосовували ІГ, СУ і РП (в прототипі застосовували ртутно-крапельний електрод). Використання таких електродів обумовлено високою хімічною і електрохімічної стійкістю графіту, широкої областю робочих потенціалів, а й простотою механічного відновлення поверхні і вимогами техніки безпеки. В РП електроді значно зменшується витрата ртуті, тому що ртуть токсична.
Максимальне значення реєстрованого струму спостерігається у ІГ електрода. СУ і РП електроди і придатні до використання, однак через велику залишкового струму вони виявилися менш зручними в роботі, ніж ІГ електрод. ІГ електрод вперше було використано для визначення ренію і ренію в присутності молібдену.
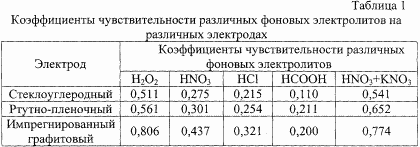
У прототипі описано використання в якості фону 4 М розчину фосфорної кислоти. У цих умовах можливе визначення тільки великих кількостей ренію (~ 10 -2%). При визначенні мікрокількостей ренію в цих умовах необхідно його виділяти зі складних складів, так як більшість супутніх елементів є заважають (наприклад, молібден, вольфрам і мідь). Пропоновані в заявляється винахід фони 1 М Н 2 О 2, або 0,5 М HNO 3, або 1 М НСl, або 0,5 М НСООН, або 1 М HNО 3 з додаванням 0,1 г KNO 3 дозволяють визначати реній з хорошою відтворюваністю. Використання фонів 0,5 М НNО 3 і 1 М НСl ускладнене тим, що при визначенні ренію спостерігався досить великий залишковий струм, а при використанні фонів 1 М Н 2 O 2 і 0,5 М НСООН неможливо визначати реній в присутності молібдену, так як на цих фонах аналітичний сигнал молібдену заглушає аналітичний сигнал ренію. Найвищий коефіцієнт чутливості спостерігався на тлі 1 М НNО 3 c додаванням 0,1 г КNO 3. Використання цього фону і дозволяє завдання спільного визначення ренію і молібдену. Межа виявлення становить 10 -6 -10 -2% (в прототипі 10 -3 -10 -2%).
Результати використання різних електродів на різних фонах наведені в табл. 1. З табл.1 видно, що у ІГ електрода найвищі коефіцієнти чутливості. Та ж картина спостерігається, якщо визначення ведеться на тлі 1 М НNO 3 з додаванням 0,1 г КNO 3, крім того, на цьому тлі можна кількісно визначати реній в присутності молібдену. Таким чином, нами було запропоновано визначення ренію і ренію в присутності молібдену на ІГ електроді і на тлі 1 М HNO 3 c додаванням 0,1 г КNO 3.
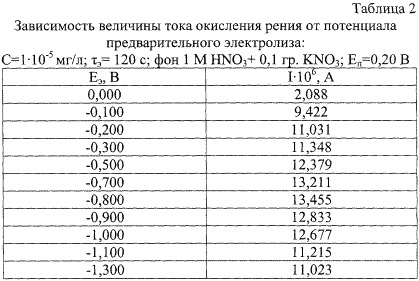
Іншою відмітною ознакою є встановлені умови електрохімічного накопичення: потенціал електролізу Е е = (- 0,7) - (- 1,0) В. Досвідчені дані показали залежність струму окислення ренію від E е (табл.2). Величина анодного струму збільшувалася і досягала максимального значення в області потенціалів (-0,7) - (- 1,0) В. Використання попереднього електролізу при значеннях потенціалу -0,8 ± 0,1 В дозволяє реєструвати вольтамперограмме з чітко вираженим максимумом. Це дозволяє підвищити точність і роздільну здатність способу.
Час попереднього електролізу ( ![]() е) вибирають в залежності від концентрації речовини. Максимальне значення величини струму окислення досягається при
е) вибирають в залежності від концентрації речовини. Максимальне значення величини струму окислення досягається при ![]() е, рівному 120-150 с. при
е, рівному 120-150 с. при ![]() е <120 знижується чутливість визначення і збільшується помилка визначення, а при
е <120 знижується чутливість визначення і збільшується помилка визначення, а при ![]() е> 150 знижується експресному.
е> 150 знижується експресному.
Важливим для визначення ренію є вибір швидкості розгортки потенціалу. Оптимальною є швидкість 30-50 мВ / с. Збільшення швидкості більше 50 мВ / с збільшує чутливість, але при цьому зростає залишковий струм і зменшується роздільна здатність способу. Використання швидкості 30 мВ / с істотно знижує величину анодного струму і знижується чутливість визначення ренію.
Таким чином, встановлені умови вперше дозволили кількісно визначати реній і реній в присутності молібдену на основі реакції електроокислення. Для підвищення чутливості визначення використовували попереднє концентрування ренію на поверхні графітових електродів. Пропонований вольтамперометрических спосіб дозволив істотно поліпшити метрологічні характеристики аналізу ренію, підвищити чутливість визначення (1 · 10 -6 мг / кг), що на 3-4 порядки нижче в порівнянні з прототипом, час аналізу не перевищує 120-150 з проти 30 хвилин. Визначенню не заважають молібден, вольфрам і мідь, які є супутніми елементами.
Як прототип обраний метод визначення ренію по вольтамперной кривою електровідновлення Re (7 +) ---> Re (4+). Нами запропоновано визначення ренію методом ІВА, при якому проводиться електроконцентрірованіе ренію на графітовому електроді з подальшим окисленням осаду. Аналіз був виконаний на приладі СТА-1 (Томськ, Росія). Обраний нами метод дозволяє значно розширити діапазон визначуваних концентрацій з 10 -3 -10 -2 до 10 -6 -10 -2%), а й дозволяє спростити апаратурне оформлення процесу. Крім того, даний спосіб дозволяє визначати реній в присутності молібдену, що виносяться пробоподготовки проби до аналізу.
Приклади конкретного виконання
Приклад №1.
Вимірювання були проведені на штучних сумішах. 10 мл фонового електроліту поміщають в кварцовий стаканчик. Не припиняючи перемішування, проводять електроліз розчину за умови: Е е = -0,800В, ![]() е = 120 с. Знімають вольтамперную криву електроокислення при швидкості розгортки 40 мВ / с, починаючи з потенціалу Е поч = 0,000 В. Відсутність піків свідчить про чистоту фону. Потім додають 0,05 мл стандартного зразка (СО) ренію і проводять електрохімічне концентрдрованіе осаду при аналогічних умовах. Пік для зазначеної концентрації речовини реєструють в діапазоні потенціалів від 0,150 до 0,250 В (щодо нас.х.е.). Робили 0,05 мл добавку СО ренію і знову реєстрували аналітичний сигнал. За різницею струмів піків ренію вираховували концентрацію ренію в розчині. Визначення ренію в присутності молібдену ведеться аналогічно, тільки в фоновий електроліт додається молібден (від 0,05 до 5 мл СО молібдену). Встановлено, що при 100-кратному надлишку молібдену (у порівнянні з ренієм) реній можна визначити кількісно. СО ренію отримували шляхом розведення 0,05 г порошку чистого ренію в 50 мл розчину, що містить 25 мл концентрованої HNO 3 і трідістіллірованную воду. СО молібдену отримували таким же чином. Фоновий електроліт отримували шляхом розведення концентрованої азотної кислоти (10 мл конц. НNO 3 в мірній колбі на 100 мл) і додавання 0,1 г КNO 3. Похибка вимірювань становить близько 1-5%.
е = 120 с. Знімають вольтамперную криву електроокислення при швидкості розгортки 40 мВ / с, починаючи з потенціалу Е поч = 0,000 В. Відсутність піків свідчить про чистоту фону. Потім додають 0,05 мл стандартного зразка (СО) ренію і проводять електрохімічне концентрдрованіе осаду при аналогічних умовах. Пік для зазначеної концентрації речовини реєструють в діапазоні потенціалів від 0,150 до 0,250 В (щодо нас.х.е.). Робили 0,05 мл добавку СО ренію і знову реєстрували аналітичний сигнал. За різницею струмів піків ренію вираховували концентрацію ренію в розчині. Визначення ренію в присутності молібдену ведеться аналогічно, тільки в фоновий електроліт додається молібден (від 0,05 до 5 мл СО молібдену). Встановлено, що при 100-кратному надлишку молібдену (у порівнянні з ренієм) реній можна визначити кількісно. СО ренію отримували шляхом розведення 0,05 г порошку чистого ренію в 50 мл розчину, що містить 25 мл концентрованої HNO 3 і трідістіллірованную воду. СО молібдену отримували таким же чином. Фоновий електроліт отримували шляхом розведення концентрованої азотної кислоти (10 мл конц. НNO 3 в мірній колбі на 100 мл) і додавання 0,1 г КNO 3. Похибка вимірювань становить близько 1-5%.
Приклад №2. 0,1 г порошку каталізатора, що містить реній, розчиняли в 15% HNO 3 в колбі на 100 мл протягом 15-20 хвилин при перемішуванні. 10 мл фонового електроліту поміщали в кварцовий стаканчик, додавали аликвотную частина 1-1,5 мл отриманого розчину каталізатора. Знімали вольтамперную криву електроокислення ренію. Робили добавку СО ренію 1 мл і знову реєстрували аналітичний сигнал. За різницею струмів піків ренію вираховували концентрацію ренію в розчині. Пік струму ренію реєструвався при потенціалі Е = 0,200 В. Концентрація ренію склала ~ 65%. СО ренію і фоновий електроліт готується так само, як в прикладі №1.
Таким чином, вперше встановлена здатність кількісного аналізу ренію по піках окислення його на ІГ електроді (в прототипі кількісне визначення ренію проводять по хвилях відновлення на ртутному краплинному електроді). Значно підвищилася чутливість визначення (більш ніж на 2-3 порядки). Умови, які використовуються в прототипі, не дозволяють аналізувати реній в присутності молібдену.
Запропонований спосіб простий, виключає використання токсичної ртуті, не вимагає великих трудовитрат, великої кількості реактивів і може бути застосований в будь-який хімічної лабораторії, які мають комп'ютеризовані аналізатори типу СТА, ТА або полярограф. Запропонований спосіб може бути використаний для визначення ренію і ренію в присутності молібдену в рудах і рудних концентратах.
Спосіб визначення ренію і ренію в присутності молібдену методом інверсійної вольтамперометрії.
ФОРМУЛА ВИНАХОДУ
Спосіб визначення ренію і ренію в присутності молібдену методом інверсійної вольтамперометрії, що полягає в тому, що реній переводять з проби в розчин і проводять вольтамперометрических визначення, що відрізняється тим, що проводять накопичення ренію на импрегнірованого графитовом електроді в перемішувати розчині протягом 120-150 с при потенціалах електролізу (-0,7 ÷ -1,0) в відносно насиченого хлорідсеребряного електрода на тлі 1 М HNO 3 з додаванням 0,1 г КNO 3 з подальшою реєстрацією анодних піків в накопичувальному режимі зйомки вольтамперограмм при швидкості розгортки потенціалу 30-50 мВ / з і концентрацію визначають по висоті піку в діапазоні потенціалів 0,150 - 0,250 в методом добавок атестованих сумішей.
Версія для друку
Дата публікації 14.03.2007гг




Коментарі
Коментуючи, пам'ятайте про те, що зміст і тон Вашого повідомлення можуть зачіпати почуття реальних людей, проявляйте повагу та толерантність до своїх співрозмовників навіть у тому випадку, якщо Ви не поділяєте їхню думку, Ваша поведінка за умов свободи висловлювань та анонімності, наданих інтернетом, змінює не тільки віртуальний, але й реальний світ. Всі коменти приховані з індексу, спам контролюється.