|
Як Ви напевно знаєте риби не літають і не ходять - вони плавають. І природно живуть у воді. Яка ж це вода - в якій живуть риби? Які у неї параметри і властивості? Яка власне кажучи повинна бути вода в акваріумі для Ваших рибок? Про це та багато іншого ми розповімо в цьому розділі.
Нам всім відомо, що вода може бути різної якості і володіти різними властивостями. Ну звичайно за винятком дистильованої води. У різних природних умовах свої параметри води. Будь-який живий організм на протязі всього свого життя нерозривно пов'язаний з навколишнім середовищем, що впливає на її зовнішній вигляд, будова тіла, особливості поведінки. Риби, будучи мешканцями водного середовища, відчувають на собі вплив таких чинників, як температура, світло, концентрація кисню і вуглекислого газу, осмотичний тиск, кислотність, жорсткість і сольовий склад води. Нижче ми познайомимося з усіма перерахованими вище параметрами докладніше.
Сама вода є життєвим простором акваріумних риб і рослин і в залежності від своїх властивостей сприяє розвитку в них життєвих процесів або гальмує їх. Вона містить різні речовини, що додають їй такі цікаві для акваріума властивості, як колір, прозорість, запах, а також значення жорсткості DH і водневого показника PH.
Для акваріума придатна чиста, прозора, що містить всі необхідні для життя рослин речовини водопровідна вода з DH = 5-20 градусів, KH = 2-15 градусів, PH = 6,5-7,5.
Кожному аквариумисту в першу чергу повинна бути відома, принаймні, жорсткість води в його домашньому водопроводі. А як дізнатися інакше, відповідну чи воду він наливає в акваріум для своїх вихованців? Взагалі-то кажучи, можна зателефонувати на водопровідну станцію і отримати загальні відомості з цього питання. Але в даний час у всіх спеціалізованих магазинах є в продажу тести, за допомогою яких Ви можете без праці зробити виміри Вашої води.
Отже, почнемо розбиратися докладніше, які параметри є у води.
КИСЛОТНІСТЬ ВОДИ (водневий показник) PH
Будь-які типи води ми розрізняємо за змістом кислот і підстав. Показник PH і є міра вмісту кислоти або підстави. Кислотність води дуже впливає на біохімічні і біологічні процеси і має важливе значення для риб. Іони в воді є носіями кислотних або лужних властивостей. Якщо лужні і кислотні іони містяться в ній в рівних кількостях, то вода реагує "нейтрально", як і відбувається (або принаймні має відбуватися) з дистильованою водою. У будь-якій воді міститься певна кількість молекул H2O, розділених на H + - катіони (позитивно заряджені іони водню) і OH - аніони (негативно заряджені іони гидроокислах). Загальний вміст H + і OH- іонів в літрі води має постійний показник: 10-14 моль / літр (моль - молекулярна вага в грамах), виміряний при 25 градусах С. Коли концентрації обох іонів рівні, зміст кожного з них становить 10 -7 моль / літр. Отже, нейтральна вода має концентрацією водневих іонів 10 -7 грамів на літр, тобто в ній містяться 0,0000001 м Н-іонів і рівно стільки ж ОН-іонів. Складно і не наочно, чи не так. Це число називають показником PH (Pondus Hydrogenii). Саме для наочності пишуть повністю не його, а тільки логарифм водневого показника без негативного знака, тобто просто "7". І відповідно водневий показник нейтрального середовища скорочено позначається як "PH 7". У кислому воді цей показник нижче, ніж 7; в лужному вище, ніж 7.
Залежно від кислотності вода класифікується наступним чином:
- PH = 1-3 сильнокислая вода
- PH = 3-5 кисла вода
- PH = 5-6 слабокисла вода
- PH = 6-7 дуже слабокисла вода
- PH = 7 нейтральна вода
- PH = 7-8 дуже слаболужна вода
- PH = 8-9 слабощелочная вода
- PH = 9-10 лужна вода
- PH = 10-14 сильнощелочной вода
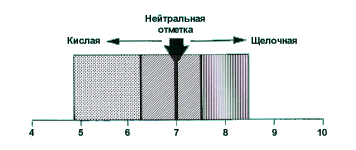 |
| Більшість рослин добре розвивається у воді, чий показник PН знаходиться на нейтральній точці (7.0). При показниках нижче 5,0 і вище 8,5 вони найчастіше перестають рости або навіть гинуть. |
Для відомості кислотність водопровідної води, а також води в проточних водоймах наближається до PH = 7.
Слід також врахувати, що дисоціація молекул води, а разом з нею і PH залежать від температури. Цей факт часто не береться до уваги навіть досвідченими акваріумістів. Тим часом, якщо виміряний при 18 градусах С PH = 7, то таку воду не можна вважати нейтральною, так як нейтральної реакції при цій температурі відповідає інше значення PH.
Водневий показник має важливе общебиологическое значення, в зв'язку з чим в процесі еволюції у більшості живих організмів виробився ряд механізмів, що забезпечують відносну сталість цього показника в клітці. Роль цього фактора визначається в першу чергу його впливом на активність ферментів і стан інших білкових молекул. Крім того, оскільки більшість реакцій в клітинах протікає у водному середовищі, надлишок або недолік іонів може суттєво впливати на перебіг також різних неферментативних реакцій. Сказане є основною причиною того, що більшість клітин, що належать різним організмам, здатне жити у вузькому діапазоні PH - від 6,0 до 8,0. Однак навіть акваріумісти зазвичай знають, що багато риби цілком безболісно переносять набагато більш значні відхилення від нейтральної реакції води. Пояснюється це тим, що організм має цілих ряд буферних систем, що згладжують різкі коливання PH середовища ..
Буферними властивостями володіють не тільки рідини організму. Значну роль в забезпеченні відносно стабільною кислотність прісних вод відіграє їх карбонатная система. Вуглекислий газ не тільки розчиняється у воді, але, вступивши в реакцію з нею, утворює слабку кислоту HCO3. Присутність у воді солей підсилює її буферні властивості, в зв'язку з чим однакове підкислення м'якою і жорсткою води викличе в першому випадку значно більше помітний зсув PH. Ще більш сильними, ніж у жорсткій води, буферними властивостями, або, як кажуть, ще більшою буферної ємністю, володіє морська вода.
Активна реакція води в значній мірі залежить від інтенсивності фотосинтезу і заселеності водойми рослинними організмами. У процесах фотосинтезу, що протікають на світлі, рослини споживають вуглекислий газ, що викликає підвищення PH. Вночі PH знижується, що пов'язано не тільки з відсутністю фотосинтезу, а й з виділенням CO3 при диханні рослин. Все це призводить до дуже значних коливань активної реакції середовища в водоймі протягом доби. Особливо великі ці коливання в водоймі з великим вмістом рослин. Щоб знизити різкі коливання кислотності води, рекомендується постійна аерація води повітрям. Про це ми детально розповімо в розділі: Аерація і фільтрація.
Практична порада:
Щоб знизити PH води, тобто зробити її більш кислої, можна додати в неї торф, взяти не височинах. Можна також додати відфільтрований екстракт, отриманий після кип'ятіння торфу. Будьте уважні, тому що надлишок торфу може виявитися шкідливим, оскільки в ньому міститься багато дубильних речовин. Лужну воду можна теж підкислити, додавши в неї біфосфат натрію.
Практична порада:
Щоб підвищити PH води, тобто зробити її більш лужною, можна додати в неї звичайної питної соди. Ну а щоб подщелочив кислу воду, потрібно додати трохи бікарбонату натрію або змішати кислу воду з лужною водопровідною водою, тобто розбавити. Останній спосіб найбільш прийнятний і вигідний, тому що при додаванні свіжої водопровідної води в воду потрапляє безліч природних гумінових кислот і зміна PH відбувається не так різко. Ще варто запам'ятати, що для утримання акваріумних риб не годиться сильнокислая, кисла, лужна і сильнощелочной вода. Вода повинна бути або дуже слабокислою, або нейтральною, або дуже слаболужною. Можна також скористатися фірмовими препаратами для зменшення PH - ми говоримо саме про зменшення тому цього домогтися набагато важче, ніж підвищити PH. Так ось будьте уважні при використанні PH down, тому що останні часто виготовляються на базі ортофосфорної кислоти. А як відомо з практики ця кислота зберігає PH на рівні близько 6.5, природно в залежності від того, скільки Ви використовували кислоти. На превеликий жаль, так саме нещастя для всіх акваріумістів, використання ортофосфорної кислоти має побічний ефект - підйом рівня фосфатів у акваріумі. А як ми знаємо з практики фосфати у воді стимулюють зростання найпростіших водоростей. Ще один спосіб зменшення PH - це використання соляної кислоти. Точна кількість кислоти, що додається в воду, буде завжди залежати від буферної ємності води. Попросту Ви додаєте кислоту до тих меж, коли буде вичерпано весь буфер води. Як тільки Ви цього досягнете то згодом зменшувати PH буде легко. Тільки пам'ятайте, що вода з низькою PH має більш меншу буферну ємність, ніж вода з підвищеною PH. А про буфері води Ви вже знаєте, читали вище. Так що робіть висновки. Будьте уважні з застосуванням цього методу, тим більше він пов'язаний з використанням кислоти - шкільну хімію напевно пам'ятаєте, з кислотами треба бути обережними.
Практична порада:
Якщо Ви виявили, що PH води у Вашому акваріумі різко змінився в одну або іншу сторону, не в якому разі не додавайте в воду відразу велику кількість соди або торфу. Запам'ятайте: Різка зміна кислотності води може призвести до загибелі риб. Все необхідно робити поступово. І ще з цього ж приводу. Щоб уникнути різкої зміни PH міняйте воду в акваріумі не великими порціями. Краще потроху і частіше, ніж рідше і відразу більше половини акваріума!
Тепер перейдемо до не менш важливого параметру води - її жорсткості.
Жорсткість води (DH)
Жорсткість води - є одним з найважливіших параметрів прісної води, від якого залежить можливість утримання і розведення в ній риб і культивування рослин в акваріумі. Слід зазначити, що її значення для акваріумних риб і рослин можуть значно відрізнятися від значень в природних водоймах, тому що риби і рослини володіють величезною пристосованість до умов навколишнього середовища, особливо в процесі зміни поколінь. Будь-яка прісна або солона вода з природних водойм містить більшу або меншу кількість іонів кальцію. Це один з найнеобхідніших елементів: у водних ракоподібних та молюсків він забезпечує твердість панцира або раковини, у риб кісткової системи. Іони кальцію відіграють також важливу роль в регуляції осмотичного тиску, про який ми розповімо нижче, і багатьох інших процесів в організмі. Так, у деяких риб зміст Ca в крові залежить від ступеня зрілості статевих залоз.
Відповідно до прийнятої у нас системі стандартизації, жорсткість висловлюють в ммоль-еквівалентах іонів кальцію (Ca ++) або магнію (Mg ++), що містяться в 1 літрі води. 1 ммоль-екв. відповідає змісту в воді 20,04 мг Ca ++ або 12,16 мг Mg ++.
У акваріумний практиці жорсткість позначають в градусах. Одному градусу жорсткості (російській або німецькому) відповідає зміст 10 мг оксиду кальцію (CaO) або 7,19 мг окису магнію (MgO) в 1 літрі води і він дорівнює 0,35663 ммоль-екв.
Жорсткість поділяють на тимчасову (карбонатну) і постійну (некарбонатную). Карбонатна жорсткість обумовлена присутністю гідрокарбонатів кальцію і магнію. При кип'ятінні гідрокарбонати руйнуються, а іони Ca2 + і Mg2 + випадають в осад у вигляді малорозчинних карбонатів. З плином часу частина випали в осад карбонатів знову розчиняється, особливо в лужній воді з показником PH = 8,3, що призводить до підвищення тимчасової жорсткості. Жорсткість, що зберігається після кип'ятіння води, називається постійною.
В основному всі тести для визначення жорсткості води зроблені для вимірювання жорсткості в градусах. Не будемо і ми тут розписувати в інших одиницях виміру, запишемо відразу в градусах.
Отже, в залежності від жорсткості вода підрозділяється:
Дуже м'яка вода
|
від 0 до 4 ° dН
|
М'яка вода
|
від 5 до 8 ° dН
|
Вода середньої жорсткості
|
від 9 до 12 ° dН
|
Досить жорстка вода
|
від 13 до 18 ° dН
|
жорстка вода
|
від 19до 30 ° dН
|
Дуже жорстка вода
|
від більш 30 ° dН
|
У літературі з акваріумістики найчастіше при вказівці жорсткості використовують "німецькі градуси жорсткості". Нижче наведена таблиця перекладу з німецьких градусів в градуси інших країн і навпаки.
|
Ньому.
° dН
|
Англ.
° еН
|
Франц.
° fН
|
Америк.
° usН
|
СНД ° suН
|
| 1 ньому.
градус
|
1,00
|
1,25
|
1,78
|
17,8
|
7,15
|
| 1 англ.
градус
|
0,798
|
1,00
|
1,43
|
14,3
|
5,70
|
| 1 франц.
градус
|
0,560
|
0,702
|
1,00
|
10,0
|
4,0
|
| 1 америк.
градус *
|
0,056
|
0,070
|
0,10
|
1,0
|
0,40
|
| 1 рус.
градус
|
0,14
|
0,111
|
0,078
|
0,0078
|
1,00
|
Дані в ppm (раrts per million) за умови, маса 1 літра води дорівнює 1 кг.
Жорсткість природних вод може варіюватися в досить широких межах і протягом року непостійна. Збільшується жорсткість через випаровування води, зменшується в сезон дощів, а також в період танення снігу і льоду. Найбільшою твердістю відрізняються води морів і океанів, а також водойм з грунтом, що складається з кальцієвих порід. Найменш жорстка вода міститься в водоймах, які харчуються виключно атмосферними опадами (за умови, якщо в їх грунтах не міститься кальцій), в водоймах тундри і тайги, в лісових водоймах і в річках, що протікають в місцевостях з торф'яними грунтами.
Практична порада:
Зверніть увагу є не попередній абзац вгорі - даний природний спосіб можна використовувати і в акваріумному господарстві.
Щоб утримувати і розводити акваріумних риб, потрібно підтримувати певну жорсткість води. Якщо в якості грунту використовувати крупнозернистий пісок і річкову гальку, тоді вода акваріума буде мати більш-менш постійну жорсткість. Треба запам'ятати і те, що в акваріумах, де містяться риби і молюски, жорсткість поступово знижується, адже кальцій витрачається на побудову молюсками своїх раковин, він засвоюється рослинами і рибами.
Які ж є способи зниження жорсткості:
Практична порада:
1. Перш за все в акваріум можна додавати дистильовану, дощову або талу воду.
2. Можна використовувати такі акваріумні рослини, як елодея і роголістнік.
3. За допомогою виморожування. Воду наливають у низький таз і ставлять на мороз або в морозильник. Після того, як вода наполовину висоти посудини замерзне, пробивають лід, воду виливають, а лід розтоплюють.
4. Шляхом змішування з більш м'якою водою. Це теж ясно.
5. Шляхом кип'ятіння води. Воду кип'ятять протягом години в емальованому посуді. Потім охолоджують і зливають 2/3 верхнього шару, у якого жорсткість буде знижена за рахунок зниження тимчасової жорсткості.
Кілька способів підвищення жорсткості:
Практична порада:
1. Шляхом кип'ятіння. Воду кип'ятять, як описано вище, але використовують нижній шар.
2. Шляхом змішування з більш жорсткою водою.
3. Додавання невеликих шматочків вапняку, крейди, мармурової крихти, черепашок, кольорового скла.
4. Шляхом додавання в воду хлориду магнію і кальцію, соди.
5. Додавання в акваріум раковин рапанів, коралової крихти (необхідно тривало виварити)
ЕЛЕКТРОПРОВІДНІСТЬ (мікросіменс)
Вирушаючи в подорож по тропіках, кожен професіонал неодмінно бере з собою електронний тестер для вимірювання електропровідності: на світлі дуже мало вод, чистих настільки, щоб вони не проводили електрику. Але в Південній Америці вони зустрічаються все-таки досить часто! Щоб вода проводила електрику, в ній повинні міститися іони (електрично заряджені частинки). Електропровідність води визначає також "осмотичний співвідношення" (вміст електроліту) в акваріумний воді. Осмотичний тиск має вирішальне значення для біологічних показників нерестової води. У більшості випадків розмноження риб вдається лише тоді, коли штучні умови наскільки можливо наближені до природних. У тропіках, на батьківщині акваріумних риб, вода найчастіше дуже м'яка і бідна мінеральними солями. Як уже згадувалося вище про жорсткість води, в басейні Амазонки нерідко зустрічаються настільки екстремальні водні показники, що тільки дивуєшся, як риби взагалі можуть там існувати, - наприклад, при показнику PН 4,5 - 4,9. Як відомо, в цій воді живе, зокрема, червоний неон (Рaracheirodon axelrodi) і аж до самих останніх років цю маленьку перлину акваріумістики ніяк не вдавалося змусити розмножуватися в наших умовах, як і деякі види расбори з Південно-Східної Азії. Досягнуті в недавній час успіхи в цій галузі пов'язані в першу чергу з науковими висновками про взаємозв'язок між електропровідністю акваріумний води і осмотичним тиском. Електропровідність води вимірюється за допомогою маленького кишенькового приладу: транзисторного тестера. Цей прилад коштує відносно недорого і дає зацікавленій аквариумисту точні свідчення.
 |
Електронні тестери провідності (в даному випадку з цифровим індикатором) за розміром досить малі, а тому зручні. Вони розроблені спеціально для акваріумістів різними фірмами: Tunze, Dupla, Stein, Bischof і іншими. |
Визначати електропровідність слід при 20 ° С. Якщо вимір треба провести на відкритому повітрі, де немає можливості довести воду до цієї температури, то треба задати дійсну температуру. Тоді результат виявиться, наприклад, нS26. Температура води має вирішальний вплив на результат. Ідеальні для розмноження риб показники від 25 до 140 Нs. Але слід підкреслити ще раз, що дистильована вода хоч і може мати 0 ° жорсткості, але майже ніколи 0 Нs електропровідності. Практика показує, що градуси провідності дистильованої води завжди досить високі. Якщо заселити риб в резервуар, де вода має інші показники, можуть виникнути проблеми. Тому при занадто різких змінах проводности акваріумісти з обережності пересаджують виробників поступово. Таким чином їм можна допомогти пристосуватися до нових життєвих умов. За своєю природою, риби, що походять з дуже бідних мінералами вод, для виведення молодняку потребують такої ж воді, навіть якщо їхні збори поколінь містилися в воді більш жорсткою, а значить - багатою мінералами. Причина цього - структура риб'ячої яйцеклітини. Ікринки, як і спермії, складаються з клітин, укладених в дуже тонку оболонку, так звану мембрану. Клітини містять, зокрема, воду, а в ній знаходяться мінеральні речовини. Сама ікринка теж оточена водою, і в ній знову-таки розчинені мінеральні солі. Таким чином, тут стикаються один з одним два елементи, розділені однієї тільки згаданої вище тоненькою мембраною і здаються однаковими, але насправді часто не є такими.
 |
 |
 |
| Приклад, який повинен роз'яснити дію осмосу на ікру: намагаючись пристосуватися до концентрації внутрішнього і зовнішнього розчинів, яйце може роздутися або стиснутися. І те, і інше руйнує здатність до розвитку, робить ікринку непридатною для розмноження. |
Вище вже говорилося про те, що визначення електропровідності і результат вимірювань залежать від температури. Як тільки температура підвищується хоча б на 1 ° С, яка вимірюється величина теж збільшується приблизно на 2%. Найчастіше її перераховують по відношенню до 20 ° С. Як це робиться, ви можете зрозуміти з таблиці.
| Температура води в ° С при вимірюванні
|
Коефіцієнт температури по відношенню до 20 ° С
|
| 15
|
1,132
|
| 16
|
1,095
|
| 17
|
1,071
|
| 18
|
1,046
|
| 19
|
1,023
|
| 20
|
1,000
|
| 21
|
0,979
|
| 22
|
0,958
|
| 23
|
0,937
|
| 24
|
0,919
|
| 25
|
0,901
|
| 26
|
0,840
|
| 27
|
0,810
|
| 28
|
0,790
|
| 29
|
0,770
|
| 30
|
0,750
|
Тепер розглянемо ще один показник води:
СОЛЬОВИЙ СКЛАД І РЕГУЛЮВАННЯ осмотичний тиск
Однією з основних проблем усіх водних мешканців, незалежно від складності їх організації, є регуляція осмотичного тиску. Осмотичний тиск розвивається в результаті дифузії молекул води через напівпроникну мембрану живих клітин. В його основі лежить властивість мембран вибірково пропускати молекули одних речовин і затримувати молекули інших.
При різної концентрації солей по обидва боки мембрани, наприклад всередині клітини і поза нею, дифузія молекул води в область більшої концентрації солей зростає. Так як концентрація розчинних речовин і білків в клітині більше, ніж в прісній воді, прісноводні організми змушені проробляти величезну роботу з видалення надлишку проникаючої в їхнє тіло води.
Одним з еволюційних пристосувань, спрямованих на обмеження проникнення води в тканини прісноводних риб, є менша, ніж у морських риб, концентрація солей в їх крові і тканинних рідинах. Крім того, прісноводні риби мають розвинені нирками, що забезпечують видалення надлишку води з організму. Сеча цих тварин містить менше солей, ніж кров і тканинні рідини.
Досить часто функція розчинених у воді солей зводиться до їх непрямого впливу на риб через харчові ланцюги. До основних мінеральних компонентів середовища відносяться фосфорні і азотні солі. Це пов'язано з тією роллю, яку в живих клітинах відіграють молекули, що містять атоми фосфору й азоту. Менше значення мають калій і кальцій, а також сірка і магній. В останньому, крім тварин, величезну потребу відчувають рослини, так, як цей елемент абсолютно необхідний для біосинтезу хлорофілу. Дія солей посилюється з підвищенням температури, що пов'язано зі зростанням інтенсивності обмінних процесів. У менших кількостях, але не в меншій мірі необхідні так звані мікроелементи - кобальт, марганець, мідь, цинк, бор, йод, кремній і деякі інші.
На рибах болісно відбивається надмірний вміст у воді солей кальцію і заліза. Навіть незначна домішка останніх викликає у дорослих риб захворювання очей, а у малюків - поразка зябер, супроводжуване масовою загибеллю.
Багато речовин, розчинені у воді, можна віднести до отруйних або шкідливим. Це сірководень, вуглекислий газ і аміак - природні продукти, які утворюються в водоймах, а також сполуки важких металів, неорганічні і органічні продукти стоків промислових підприємств. Остання група отрут в умовах акваріума не зустрічається.
Кількість солей в прісній воді мізерно (не перевищує десятих часток грама на літр) і змінюється в прісноводому акваріумі в залежності від грунту, вмісту продуктів розпаду, випаровування води. Зміни ці невеликі, і риби і рослини легко до них пристосовуються. В окремих випадках акваріумісти навмисно кілька підвищують солоність додаванням кухонної солі.
Тепер трохи про світло, тобто про освітленості води.
освітленість ВОДИ
Далі хотілося б трохи зупинитися на такому параметрі, як осещённость води, але зовсім коротко, тому що детально про це Ви можете дізнатися з розділу: Освітлення в акваріумі.
Тут ми тільки хотіли торкнутися цього питання в загальних рисах.
І так:
Існування життя на Землі можливо завдяки енергії Сонця. Світло являє собою один з найбільш мінливих і в той же час самий регулярний в своєму впливі фактор зовнішнього середовища. Він є необхідною умовою для існування рослинних організмів, а також для поїдають їх тварин. Рибам світло необхідне для орієнтування в просторі, знаходження їжі і своєчасної реакції на наближення хижака.
Для тварин, що мешкають у воді, основним джерелом світла є сонячна радіація, яка надходить з атмосфери в поверхневі шари води. Кількість проникаючого світла визначається не тільки часом доби або прозорістю атмосфери, але і станом водної поверхні: гладка поверхня відбиває значно менше сонячних променів. Певна частина сонячної радіації поглинається водою, причому менше інших поглинаються сині промені; червоні промені поглинаються значно сильніше.
Основним органом сприйняття світла у риб є очей. Велика частина риб розрізняє колір. Спектр квітів, які сприймаються рибами, багато в чому визначається екологічними особливостями місць проживання. Природно, що мешканці верхніх шарів води, як і риби мілководдя і прибережних зон, розрізняють значно більше квітів, ніж глибоководні риби. У сутінках риби сприймають тільки короткохвильові промені.
Забарвлення тіла більшості риб найтіснішим чином пов'язана з особливостями освітлення, залежними, в свою чергу, від умов місць проживання та біології тварин. Вона мінлива і в процесі індивідуального розвитку може зазнавати значні зміни. Часто вона змінюється протягом доби.
Значну роль відіграє освітленість і в розвитку риб, регулюючи статеве дозрівання і особливості статевого циклу.
Для нормальної життєдіяльності риб і рослин в акваріумі потрібно різна потреба в освітленні. На практиці тривалість світлового дня необхідна від 8 до 10 годин на добу.
Світло буває природний, змішаний і штучний. Якщо акваріум знаходиться недалеко від вікна, то він буде в повній мірі забезпечено природним світлом.
Змішане освітлення зазвичай використовується восени і взимку, а також, якщо прагнуть до декоративного ефекту або коли вирощуються переважно водні рослини.
Штучне освітлення залежить від сили освітлення з вікна і від конструкції акваріума. Для утримання, а часто і для розведення більшості різних видів риб і рослин, не має великого значення, чи буде акваріум висвітлюватися природним або штучним світлом. Однак перевага останнього в тому, що його силу легко регулювати. Освітлення акваріума сонячним світлом має свої недоліки, головний з яких - трудність регулювання інтенсивності і тривалості природного освітлення. Крім того, при установці акваріума біля вікна риби виглядають невиразно.
Інтенсивність освітлення в акваріумі повинна відповідати інтенсивності освітлення, властивої рибам і рослинам в природних водоймах. Вона регулюється дослідним шляхом. При цьому слід враховувати обсяг акваріума і кількість живих організмів, його населяють.
Тепер трохи про температуру води.
ТЕМПЕРАТУРА ВОДИ
Діапазон відомих нам температур дуже великий - від багатьох тисяч градусів на Сонце і інших зірках до близького до абсолютного нуля холоду космічного простору. В умовах біосфери Землі різниця між максимальними та мінімальними температурами значно менше і не досягає навіть декількох сотень градусів. В значно меншому інтервалі, що вимірюється кількома десятками градусів, здатні рости, розвиватися і розмножуватися більшість відомих нам живих істот. Для деяких організмів цей діапазон буває ще більш вузьким.
У водному середовищі коливання температури виражені значно менше, ніж в атмосфері, що пов'язано з високою питомою теплоємністю води. Верхньою межею для переважної більшості видів риб є +40 градусів С, а нижня межа близький до температури замерзання води, і таку температуру переносять більшість видів.
На організм риб температура впливає двояко. В першу чергу це прямий вплив, особливо істотне для риб, як тварин з непостійною температурою тіла. У більшості риб температура тіла лише на 0,5-1 градус С вище температури водного середовища. Якщо врахувати, що більшість обмінних процесів в організмі контролюється ферментами, активність яких дуже залежить від температури, то зв'язок між температурою водного середовища і інтенсивністю обміну речовин стане цілком очевидною.
Для кожного виду риб існує певний верхня і нижня межа температури води; якщо ця межа порушується, риба гине. Звичайно, бувають випадки, коли при значному зниженні температури води риби не гинуть, а просто стають млявими, однак без шкідливих наслідків (наприклад втрата здатності до розмноження, різні захворювання).
З підвищенням температури в зазначених для водного середовища межах обмінні процеси в організмі риби посилюються, що викликає збільшення споживання кисню. Відомо, однак, що з підвищенням температури розчинність в воді газів і, зокрема кисню, зменшується. Таким чином здійснюється опосередкований вплив підвищення температури на риб, коли всупереч зростаючим потребам організму забезпечення киснем знижується, і тварини в кінцевому підсумку гинуть від задухи. Слід зазначити проте, що посилення обміну речовин (зокрема, швидкості переварювання їжі) спостерігається лише в області оптимальних для даного виду риб температур. За перевищення певного порогу включаються різні фізіологічні та біохімічні захисні механізми, завдяки чому, наприклад, холодноводниє риби на дію високих температур відповідають зниженням інтенсивності харчування і різким зниженням активності.
Якщо пересадити риб з теплої води в холодну, у них настане шоковий стан, яке зовні проявляється в тому, що риби плавають повільно, мляво ворушачи плавцями і зябрами, або нерухомо лежать на дні. Врешті-решт вони гинуть. Якщо пересадити риб з холодної води в теплу, вони, навпаки, метушаться по акваріуму, намагаються вистрибнути з води.
Практична порада:
Щоб уникнути цього, пересаджувати риб необхідно тільки тоді, коли температура в обох судинах буде однаковою або не перевищує 2 градусів С при пересадці з більш теплої води в більш холодну і 4 градусів С - з більш холодної води в більш теплу. При пересадці мальків ця різниця повинна бути в два рази меншою. Тропічних риб взагалі не рекомендується пересаджувати з більш теплої води в більш холодну.
Температура води в значній мірі регулює такі важливі сторони життєвого циклу риб, як дозрівання статевих продуктів і розвиток заплідненої ікри. Прискорення дозрівання ікри або сперми пов'язано із загальним підвищенням інтенсивності обміну речовин. Крім того, на ці процеси впливає забезпеченість їжею самих виробників і підростаючої молоді. Цим, зокрема, пояснюється порційний нерест багатьох тропічних видів риб, молодь яких майже цілий рік може знайти собі необхідний корм.
У природі спостерігаються коливання температури води, що викликаються її денним прогревом і нічним охолодженням. Амплітуда цих коливань іноді може досягати 10 градусів С і більше. Якщо в природному водному середовищі риби можуть підніматися або опускатися в шари з оптимальною для них температурою, то в акваріумі у них така можливість відсутня. У зв'язку з цим для більшості риб амплітуда між максимальною і мінімальною температурою не повинна перевищувати 2-3 градусів С, а в період нересту - 1 градуса С. Підтримання температури на необхідному для конкретного виду або групи видів рівні є обов'язковим. Яким чином домогтися постійної температури Ви дізнаєтеся з розділу: Обігрів акваріума.
Практична порада:
Незважаючи на те, що всі риби безболісно переносять недовге перебування у воді, температура якої виявилася нижче оптимальної, не в якому разі не слід, виявивши своє упущення, прагнути до швидкого підвищення температури - досить усунути несправність, сприяючи плавному встановленню температури на необхідному рівні.
І ще один короткий рада в ув'язненні: Купуючи риб, насамперед з'ясуйте при якій температурі вони жили на колишньому місці. Знати це необхідно для того, щоб поступово привчити їх до температури води в даних умовах. Також слід чинити, набуваючи і водні рослини.
Ну і на завершення теми про властивості і параметри води, необхідно трохи розповісти про зміст у воді кисню, вуглекислого газу, сірководню та азоту.
КИСЕНЬ, ВУГЛЕКИСЛИЙ ГАЗ, сірководень, АЗОТ В ВОДІ
Засвоєння тваринами кисню і видалення вуглекислого газу настільки ж необхідно, як травлення і засвоєння їжі, і є основою всіх процесів життєдіяльності. Потреба в кисні визначається енергетичними затратами організму на рух, роботу внутрішніх органів, забезпечення потреб кожної клітини тіла. Слід розрізняти фізіологічні процеси обміну киснем і вуглекислим газом між організмом а зовнішнім середовищем (газообмін) і біохімічні процеси використання кисню і утворення вуглекислого газу в клітинах (тканинне або клітинне дихання). Газообмін - дуже важливий для організму процес, ефективність якого забезпечує в кінцевому підсумку його виживання.
І кисень, і вуглекислий газ (З3, інша назва - діоксид вуглецю) представляють собою газоообразние речовини, саме в такому вигляді вони засвоюються або виділяються наземними тваринами. Їх співвідношення в атмосферному повітрі становить в середньому 700: 1, що створює сприятливі можливості для дихання. У воді це співвідношення зовсім інше. Внаслідок обмеженої розчинності максимальний вміст кисню в воді приблизно в 20 разів менше, ніж в повітрі. Вуглекислий газ на відміну від кисню здатний не тільки розчинятися, а й реагувати з водою хімічно, утворюючи вугільну кислоту. Фізичний процес розчинення вуглекислого газу протікає головним чином в кислому середовищі. У нейтральній і особливо лужному середовищі значна частина діоксиду вуглецю вступає в хімічні реакції з містяться у воді солями.
Найгірша (в порівнянні з наземними тваринами) забезпеченість водних тварин киснем певною мірою компенсується легкістю віддачі діоксиду вуглецю, зумовленої його хімічним зв'язуванням. Хоча таким чином і полегшується газообмін, в специфічних умовах водного середовища залишається невирішеною головна проблема - доступність кисню. Це послужило причиною виникнення самих різних пристосувань організмів.
Відомо, наприклад, що на різних стадіях свого індивідуального розвитку тварини по-різному переносять дефіцит кисню. Так, у риб, що мешкають і розмножуються в озерах з пониженим вмістом кисню, часто зустрічається дрібна ікра. Це призводить до збільшення відносини поверхні ікринки до її об'єму, що полегшує газообмін. Ікра інших риб має пристосування, що забезпечують її розвиток на багатій киснем поверхні або в товщі води. Позірна на перший погляд незрозумілих наявність у багатьох риб проточних вод придонному ікри пов'язано з набагато кращою забезпеченістю їх киснем в порівнянні з придонними зонами стоячих вод. Таким чином, для більшості риб (як і для інших водних тварин) кисень дуже часто є чинником, що лімітує їх розвиток і розселення.
Як вже говорилося, вуглекислий газ є одним з кінцевих продуктів обміну речовин живих клітин. Газообмін гідробіонтів, а також розчинений у воді вуглекислий газ повітря - основні джерела діоксиду вуглецю в водоймах. Розчинення СО3 супроводжується утворенням і дисоціацією вугільної кислоти і сприяє підкислення водного середовища. У свою чергу, поглинання СО2 рослинами в процесі фотосинтезу зменшує активну реакцію водного середовища (PH), яка при значному розвитку фітопланктону в період цвітіння водойм зміщується в лужний бік. При цьому рослини не тільки повністю споживають розчинений СО2, а й сприяють переходу гідрокарбонатів в карбонати. Рослини, на відміну від тварин, які страждають від підвищення змісту З3 в воді, відгукуються на це посиленням фотосинтезу.
Вуглекислота, або двоокис вуглецю, при розчиненні у воді утворює слабку кислоту (в літературі її часто називають також вугільної кислотою). Але акваріуміст не повинен плутати різні терміни, коли вони записані у вигляді хімічних формул: Вугілля - С (від Саrboneum, вугілля). Окис вуглецю, чадний газ - СО. Двоокис вуглецю, вуглекислий газ - СО (газ без запаху і кольору, міститься також в підгодівлі для рослин). Вугільна кислота - H 2 CO 3 (розчинена у воді двоокис вуглецю; слабка кислота).
Перший висновок: вуглекислота робить воду кислої. Це і є та сама причина, по якій на водопровідних станціях у води перед пуском її в споживчу мережу знижують кислотність. Кислота агресивна і могла б впливати на систему трубопроводів. Будь-яка природна вода містить вуглекислоту в різних кількостях, в розчиненої або пов'язаної формі. Вуглекислота зв'язується з сполуками кальцію і магнію, іншими словами: щоб у воді був кальцій, там має бути і деяка кількість вільної вуглекислоти.
Якщо вміст вуглекислоти надлишково, її називають вільної або розчиненою. Чим вище частка бікарбонату кальцію в воді, тим вище і частка зв'язаної вуглекислоти. Під добривом CO 2 в акваріумістики мається на увазі підгодівля акваріумних рослин вуглекислим газом за допомогою дифузора. Щоб засвоювати вуглекислоту, рослинам потрібно багато світла. Тільки завдяки світлу може початися процес асиміляції, а ґрунтовне поглинання CO 2 листя рослин доводять тим, що випускають крихітні бульбашки кисню. Якщо подача вуглекислоти в акваріумну воду надмірна, це позначиться на зниженні показника PН. Занадто сильний приплив вуглекислоти заважає вільному диханню риб і приносить шкоду: риби зависають прямо під поверхнею води і намагаються пропустити через свої зябра багату на кисень воду.
У порушеною акваріумному середовищі на верхній стороні листя рослин іноді з'являються вапняні відкладення. Це явище, зване "біогенним відкладенням вапна" або "бикарбонатной асиміляцією", проявляється тим сильніше, чим вище карбонатная жорсткість води при одночасному потужному освітленні. У такому випадку через нестачу вуглекислоти процес йде у зворотному порядку. Так як вільної чи розчиненої вуглекислоти немає , то рослини поглинають нижньою стороною листа бікарбонат кальцію, розчиняють всередині листа пов'язану вуглекислоту і випускають з верхньої сторони гідроокис кальцію - Са (ОН) 2. При цьому карбонатная жорсткість води зменшується, а показник PН зростає. На листках видно сіруватий наліт, і поверхня їх на дотик стає досить жорсткою (як би посипаною порошком).
Багатьом аквариумистам відомо, що в м'якій воді рослини розвиваються погано. В першу чергу це пов'язано з тим, що відсутність вапна - це відсутність амортизатора для вуглекислоти. З іншого боку, при використанні так званого добрива CO 2 цілком достатньо невеликої добавки вуглекислоти, щоб рясно підживити рослини. У нічний час процес асиміляції призупиняється, а тому підживлення рослин CO2 теж треба припинити.
Джерело кисню для акваріумних риб - водні рослини і атмосферне повітря. Якщо поверхню акваріума досить велика, а рівень постійно перемішуємо води низький, в цьому випадку значна кількість кисню надходить з повітря. Такий тип акваріума зазвичай застосовується як нерестовище; в них не повинно знаходитися велика кількість риб. У звичайному акваріумі, де поверхня води невелика, а рівень високий, атмосферного кисню надходить в воду трохи.
Для насичення води киснем існує два способи: механічний і біологічний. Перший - це аерація акваріума за допомогою компресора. Про цей спосіб ми детально розповімо в розділі: Аерація і фільтрація.
Вступник за допомогою розпилювача повітря з нижніх шарів води в акваріумі виходить на поверхню у вигляді бульбашок, при цьому вода стикається з повітрям і збагачується киснем. Другий спосіб - це виділення кисню водоростями.
При відсутності в акваріумі водних рослин, риб не вистачає кисню; в такому випадку вони тримаються на поверхні води під кутом 45 градусів і посилено хапають повітря ротом. Таке кисневе голодування часто призводить до захворювання і загибелі риб. Якщо в акваріумі надлишок рослин, він повинен добре висвітлюватися, щоб відбувався процес фотосинтезу і виділення кисню, інакше риби також можуть загинути від задухи.
Кисень повинен бути розчинений в будь-якому акваріумі в якомога більшій кількості. Кисень - це газ, чия розчинність в воді залежить від температури: чим тепліше вода, тим швидше випаровується кисень. Його не можна розглядати тільки як елемент, необхідний для життя риб: очищення води від отрут теж залежить від кисню, тому що розкладання отруйних речовин забезпечують в першу чергу кіслородозавісімие бактерії. Вода може поглинати кисень всюди, але в природних водах (річки, озера, ставки) це відбувається майже виключно на поверхні. Вода колодязів і джерел киснем тому бідна.
Якщо акваріумна вода активно збагачується киснем за рахунок подачі зовнішнього повітря, то він може витіснити наявну вуглекислоту. У літературі з акваріумістики часто використовується термін "насичення киснем".
Так, дійсно можна досягти не тільки насичення, але й перенасичення води киснем, якщо за рахунок асиміляції рослин він накопичується в надлишковій кількості. Поглинання кисню визначається температурою води. Чим холодніше вода (над точкою замерзання), тим більше кисню вона може прийняти. Це стосується і інших газів, наприклад, вуглекислого, хоча і в іншому масштабі.
У подальшій практиці Ви можете використати таку таблицю:
| Температура води в ° С
|
Насичення киснем в мг / л
|
| 0
|
14,2
|
| 6
|
12,1
|
| 12
|
10,0
|
| 18
|
9,2
|
| 24
|
8,2
|
| 26
|
8,0
|
| 28
|
7,7
|
| 30
|
7,5
|
| 32
|
7,3
|
| 34
|
7,1
|
| 40
|
6,6
|
Про що ж ця таблиця повідомляє аквариумисту? Якщо для розмноження риб або через необхідність терапії (лікування хвороби) температура води перевищує норму, відповідно потрібно збільшити і подачу кисню. Досвідчений акваріуміст дізнається по частоті дихання своїх риб, коли настав цей момент, Правда, якщо риби вдихають швидше, ніж зазвичай, не треба робити виведення виключно про нестачу кисню. У цьому можуть бути винні і інші речі, наприклад, отруєння або зяброві паразити (див. Розділ: Хвороби риб ).
Вміст кисню у воді вимірюється за допомогою індикаторів, які можна придбати в спеціалізованих магазинах.
Практична порада:
Уникнути цих неприємностей можна, якщо встановити оптимальний світловий режим, проводити аерацію води за допомогою компресора, щотижня замінювати 1/5 частина води з дна на свіжу, сифонить грунт.
У високих акваріумах без штучної аерації води в придонних шарах виникає нестача кисню. В цьому випадку не з'їдені рибами залишки їжі, опустилися на дно, не окислюються, а гниють. Це відбувається в тому випадку, якщо акваріуміст дає рибам надмірна кількість живого і сухого корму. У процесі гниття відбувається виділення сірководню, який може привести до загибелі риб. Така ж ситуація виникає і тоді, коли грунт в акваріумі складається з дуже дрібного піску, що перешкоджає проникненню кисню всередину грунту. Ознаками присутності сірководню служать потемніння верхнього шару грунту і запах тухлих яєць з дна акваріума, з якого злита вода. У разі появи у воді сірководню, необхідно регулярно аерувати акваріум повітрям; також слід замінити пісок на більший.
Азот погано розчиняється у воді і тому мало небезпечний для риб. Однак в разі надмірної аерації акваріума, під надлишковим тиском бульбашки азоту можуть накопичуватися і приводити до закупорки кровоносних судин риб. Більш небезпечні для них сполуки азоту, які є продуктами розкладання органічних речовин, таких, як залишки корму, екскременти і т.п. До таких сполук слід віднести аміак (NH3) і амоній (NH4), які можуть проникати в тканини риб. Співвідношення цих речовин залежить від кислотності води. При цьому при високому PH аміак більш отруйний, ніж амоній; при низькому вмісті кисню у воді токсичність сполук азоту збільшується. Зміст амонію в кількості 0,2 мг / л допустимо, а така ж кількість аміаку призводить до загибелі риб.
Практична порада:
При зміні води в акваріумі НЕ доливайте відразу велику кількість води, оскільки в разі підвищення рівня PH води може статися реакція, в результаті якої амоній може перейти в аміак.
Під дією нитрифицирующих бактерій аміак і амоній окислюються спершу до азотистої (HNO2), а потім до азотної (HNO3) кислоти. Солі азотної кислоти - нітрит нестійкі, але навіть мале їх кількість небезпечно для риб, так як негативно впливає на гемоглобін крові, на тканини і судинну систему риб; солі ж азотної кислоти - нітрати менш отруйні. При відсутності в акваріумі рослин, а також при перенаселення акваріума рибами відбувається надлишкове скупчення нітратів, що, в свою чергу, призводить до перетворення нітратів в нітрити.
Практична порада:
Щоб уникнути таких неприємностей слід щотижня міняти 10-15% води, а також не допускати перенаселення акваріума.
|
|









Коментарі
Коментуючи, пам'ятайте про те, що зміст і тон Вашого повідомлення можуть зачіпати почуття реальних людей, проявляйте повагу та толерантність до своїх співрозмовників навіть у тому випадку, якщо Ви не поділяєте їхню думку, Ваша поведінка за умов свободи висловлювань та анонімності, наданих інтернетом, змінює не тільки віртуальний, але й реальний світ. Всі коменти приховані з індексу, спам контролюється.