|
початок розділу
Виробничі, аматорські радіоаматорські Авіамодельний, ракетомодельного Корисні, цікаві |
хитрощі майстру
електроніка фізика технології винаходи |
таємниці космосу
таємниці Землі таємниці Океану хитрощі Карта розділу |
|
| Використання матеріалів сайту дозволяється за умови посилання (для сайтів - гіперпосилання) | |||
Навігація: => |
На головну / Каталог патентів / В розділ каталогу / Назад / |
|
ВИНАХІД
Патент Російської Федерації RU2286187
![]()
СПОСІБ КОМБІНОВАНОГО органозберігаючого лікування
ЗЛОЯКІСНИХ ПУХЛИН ОРБІТИ
Ім'я винахідника: Ліхванцева Віра Геннадіївна (RU); Будзінська Марія Вікторівна (RU); Мерзлякова Оксана Юріївна (RU); Шевчик Сергій Олександрович (RU); Лощенов Віктор Борисович (RU); Ворожцов Георгій Миколайович (RU); Кузьмін Сергій Георгійович (RU)
Ім'я патентовласника: ГУ Науково-дослідний інститут очних хвороб РАМН (RU); ГУП Москви Міжнародний Науковий і Клінічний Центр "Інтермедбіофізхім" (ГУП МНКЦ "ІНТЕРМЕДБІОФІЗХІМ") (RU)
Адреса для листування: 119021, Москва, вул. Рассолімо, 11, НІІГБ РАМН, каб.417, В.Г. Ліхванцевой
Дата початку дії патенту: 2005.04.13
Винахід відноситься до офтальмології, а саме до офтальмоонкологіі і призначене для комбінованого органозберігаючого лікування хворих із злоякісними пухлинами орбіти. Проводять орбітотомія з видаленням пухлини ad maximum, интраоперационную фотодинамічної терапії та хіміотерапію. За 3 доби до операції вводять фотосенсибілізатор Фотосенс в дозі від 0,1 до 1,0 мг / кг ваги. Безпосередньо після видалення пухлини і відмивання операційної рани від крові заповнюють порожнину фізіологічним розчином, вводять в неї циліндричний діффузорний світловод і проводять опромінення лазерним впливом з довжиною хвилі 670 нм і щільністю потужності від 120 до 800 мВт / см 2. Видаляють фізіологічний розчин. Витягають світловод. Вшивають рану. У післяопераційну періоді проводять хіміотерапію. Спосіб дозволяє добитися повноцінної деструкції пухлини, уникнути променевої резистентності і широкого ряду постлучевих ускладнень.
ОПИС ВИНАХОДИ
Винахід відноситься до офтальмології, а саме - до офтальмоонкологіі, і призначене для оптимізації лікування злоякісних пухлин орбіти.
На сьогоднішній день лікування злоякісних пухлин орбіти поділяється на два види: ликвидационное і органосохранное.
Ліквідаційні способи лікування включають екзентерацію орбіти (видалення всього вмісту орбіти). Екзентерацію орбіти протягом багатьох десятиліть розцінювали як радикальний метод лікування злоякісних пухлин орбіти [Керівництво по офтальмоонкологіі. - Під керівництвом проф. А.Ф.Бровкіной. М .: Медицина, 2002 с.112]. Вони проводяться в тих випадках, коли органосохранное лікування неможливо, наприклад, в разі поширення пухлини до вершини орбіти, коли шансів на її знищення за допомогою променевої та / або хіміотерапії терапії не залишається або вони дуже малі, і ймовірність проростання пухлини в порожнину черепа настільки висока , що на передній план виступає боротьба за життя пацієнта, а не порятунок очі, як органу зору. Показанням до екзентерація орбіти можуть бути рецидивні пухлини, резистентні до хіміотерапії і / або променевої терапії. До розряду таких належить, наприклад, ботріоідние тип ембріональної рабдоміосаркома у дорослих.
В останні роки доведено, що радикальність цього методу досить відносна. «Тривале спостереження за хворими після екзентерація орбіти показало, що переживають 1 рік після операції тільки 89%, 5 років - 63%, а 10 років - 48%. Таким чином, тривалість життя пацієнтів після цієї операції, що калічить не вище, ніж після комбінованого органосохранное лікування »[Керівництво по офтальмоонкологіі. - Під керівництвом проф. А.Ф.Бровкіной. М .: Медицина, 2002 с.112].
Але при цьому екзентерація призводить ще й до інвалідизації хворого, а й до тяжких косметичних дефектів, які істотно погіршують якість життя цього важкого контингенту хворих.
Органозберігаюче лікування полягає в застосуванні комбінації декількох видів лікування: наприклад, спосіб орбітотоміі з видаленням пухлини ad maximum, променеву терапію і хіміотерапію. У міжнародному протоколі лікування злоякісних сарком орбіти відразу після операції проводять курс хіміотерапії протягом двох тижнів, після чого підключають зовнішнє опромінення орбіти. Опромінення орбіти проводять за допомогою дистанційної гамма-терапії [Керівництво по офтальмоонкологіі. - Під керівництвом проф. А.Ф.Бровкіной. М .: Медицина, 2002 с.375].
Вибір схеми і комбінації поліхіміотерапії визначається гістогенезом пухлини. 26% злоякісних пухлин орбіти представлено мягкотканное саркомами, при яких променева терапія застосовується в якості ад'ювантної, тобто, є доповненням до хірургічного та хіміотерапевтичне видам лікування [Baker KS, Anderson JR, Link MP, et al: Benefit of intensified therapy for patients with local or regional embryonal rhabdomyosarcoma: Results from the Intergroup Rhabdomyosarcoma Study IV. J Clin Oncol - 2000 - vol.18 - pp.2427-2434].
Метою променевої терапії є постлучевая регресія залишкової пухлини (радикальна програма опромінення) або запобігання рецидиву. При цьому сумарна доза дистанційної гамма-терапії залежить від стадії неопластического процесу і коливається від 40 до 60 Гр (1,5-1,8 Гр за фракцію) [Donaldson SS, et al: Results from the IRS-IV randomized trial ofhyperfractionated radiotherapy in children with rhabdomyosarcoma: A report from the IRSG.// Int J Radiat Oncol Biol Phys - 2001 - vol. 51 - pp.718-728 - 2001; Wolden SL, Anderson JR, et al: Indications for radiotherapy and chemotherapy after complete resection in rhabdomyosarcoma: A report from the Intergroup Rhabdomyosarcoma Studies I to III.// J Clin Oncol - 1999 - vol.17 - pp.3468-3475].
Незважаючи на високу ефективність комбінованого методу лікування злоякісних сарком орбіти (5-річна виживаність досягає 93%), до 10% рабдоміосарком можуть виявитися рефракторная як до хіміо-, так і до променевої терапії [Керівництво по офтальмоонкологіі. - Під керівництвом проф. А.Ф.Бровкіной. М .: Медицина, 2002 с.112].
Цей спосіб комбінованого органозберігаючого лікування злоякісних пухлин орбіти за допомогою орбітотоміі з видаленням пухлини ad maximum, променевої терапії та хіміотерапії прийнятий за найближчий аналог пропонованого винаходу [там же, стр.375]. Він має низку переваг перед ліквідаційної екзентерація. Він дозволяє підсилити лікувальний компонент. У разі залишків пухлинних клітин в орбіті променева терапія призводить до їх загибелі. Разом з тим, у нього є деякі недоліки.
По-перше, дистанційна гамма-терапія тягне за собою ряд серйозних ранніх і пізніх ускладнень. До ранніх ускладнень відносяться постлучевая кератити, кератопатії, дерматити, іридоцикліти, нейроретинопатии [Abramson DH, Notis CM: Visual acuity after radiation for orbital rhabdomyosarcoma.// Am J Ophthalmol - 1994 - vol.11 - pp.808-809].
До пізніх ускладнень постлучевого терапії відносять країни, що розвиваються гіпоплазію або асиметрію тканин лицевої ділянки, часом вимагає реконструктивної хірургії, деформації зубів, погіршення зорових функцій в зв'язку з розвиненими катарактами і рогівковими змінами, атрофією зорового нерва [Raney RB, et al: Late complications of therapy in 213 children with localized, nonorbital soft-tissue sarcoma of the head and neck: A descriptive report from the Intergroup Rhabdomyosarcoma Studies (IRS) -II and III.// Med Pediatr Oncol - 1999 - vol.33 - pp.362-371; Merriam GR Jr, Focht EF: A clinical study of radiation cataracts and the relationship to dose.// Am J Roentgenol Rad Ther Nuclear Med - 1957 - vol.77-pp.759-789].
По-друге, променева терапія в ряді випадків призводить до розвитку друге пухлин (сарком, карцином, лейкемії) [Raney RB, et al: Late complications of therapy in 213 children with localized, nonorbital soft-tissue sarcoma of the head and neck: A descriptive report from the Intergroup Rhabdomyosarcoma Studies (IRS) -II and III.// Med Pediatr Oncol - 1999 - vol.33 - pp.362-371].
По-третє, деякі гістогенетичних типи пухлин можуть проявити резистентність до променевим механізмам деструкції [Mandell L, et al. Ra-diocurability of microscopic disease in childhood rhabdomyosarcoma with radiation doses less than 4,000 cGy // Journal of Clinical Oncology - 2001 - vol. 8 -pp. 1536-1542; Komdeur R, et al. Multidrug resistence proteins in rhabdomyosarcomas: comparison between children and adults.// Cancer - 2003 - vol.97 - №8 - pp.1999-2005].
У зв'язку з цим пошук нових, перспективних методів органосохранное лікування при злоякісних пухлинах виправданий і надзвичайно актуальне.
Фотодинамічна терапія як метод лікування злоякісних пухлин з'явився порівняно недавно. Вона активно розвивається в передових країнах світу. Суть методу полягає у введенні фотосенсибилизирующего речовини, яке вибірково накопичується в активно пролиферирующей злоякісної пухлини і подальшому променевому впливі на патологічний осередок. Терміни та режими проведення опромінення визначаються залежно від застосовуваного фотосенсибілізатора і локалізації пухлини. У офтальмоонкологіі метод тільки почав застосовуватися для лікування внутрішньоочних пухлин [Jurklies, G Anastassiou, S Ortmans, et al. Photodynamic therapy using verteporfin in circumscribed choroidal haemangioma.// British Journal of Ophthalmology. - 2003. - Vol.87. - P.84-89; Kim RY, Hu LK, Foster BS, et al. Photodynamic therapy of pigmented choroidal melanomas of greater than 3-mm thickness.// Ophthalmology. - 1996. - Vol.103. - P.2029-2036].
До справжнього моменту в клінічній онкології вже визначено ряд областей, де ФДТ високо ефективна. Так, Міністерством охорони здоров'я Російської Федерації опублікований аналіз результатів ФДТ злоякісних новоутворень шкіри, молочної залози, слизової оболонки порожнини рота, язика, нижньої губи, гортані, легенів, стравоходу, шлунка, сечового міхура, прямої кишки та інших локалізацій [Опубліковано в Інтернеті на сайті: http://www.magicray.ru/RU/lecture/L1/1.shtmll].
Аналіз результатів клінічних випробувань ФДТ дозволив визначити основні напрямки застосування ФДТ:
- При початкових стадіях раку ФДТ за радикальною програмою, розрахованою на повне вилікування; при раку шкіри (великому поверхневому, множині, при "незручних" локалізаціях на обличчі, вушних раковинах), при раку легені, стравоходу, сечового міхура (поверхнево-стелеться, множинний вузловий), геніталій.
- При далеко зайшли пухлинних процесах трахеї, великих бронхів, стравоходу, кардіального відділу шлунку ФДТ застосовується з метою реканалізації.
- У комбінованому і комплексному лікуванні при рецидивах раку шкіри, нижньої губи, мови, внутрішньошкірних метастазах і рецидивах раку молочної залози на грудній стінці, при внутрішньошкірних метастазах меланоми, як правило, в поєднанні з поліхіміотерапією.
Виявляється чітка тенденція до використання ФДТ в передопераційному періоді для зменшення обсягу резекції, під час деяких нерадикальних операцій, наприклад при пухлинах головного мозку, біліодігестівних зони, для підвищення радикалізму операції і поліпшення результатів лікування. Висловлюються припущення про те, що ФДТ може виявитися корисною в якості передопераційної підготовки при поширених формах бронхогенного раку, езофагіті Барретта, а й при пересадці червоного кісткового мозку.
ФДТ можлива з паліативної метою при великих розпадаються пухлинах для гемостазу. З огляду на нешкідливість і хорошу переносимість методу ФДТ, його можна застосовувати в поєднанні з хірургічним втручанням, променевою лікуванням і хіміотерапією. Можна не сумніватися значний економічний ефект даного методу за рахунок короткостроковість лікування переважно в амбулаторних умовах [http://www.magicray.ru/RU / lecture / L 1 / 1.shtmll.].
Ад'ювантна місцева терапія, яка проводиться після хірургічного видалення пухлини, визнана однією з найперспективніших сфер застосування ФДТ. ФДТ показана і ефективна при локалізаціях, що можуть призвести високим ризиком місцевих рецидивів і важкими ускладненнями променевої терапії. Теоретично ідеально застосовувати ФДТ в ході хірургічного втручання (інтраопераційно), оскільки максимально відкритий доступ до патологічного вогнища. Це дозволяє адекватно оцінити дозу світлового опромінення і доставити світло до тканин з високим ризиком. На сьогоднішній день областями застосування ФДТ з ад'ювантної метою і захворюваннями є: черевна порожнина після видалення злоякісних новоутворень шлунково-кишкового тракту; саркоми, розташовані забрюшинно або вражаючі кишечник і мають невеликі розміри; злоякісні гліоми; стану після радикальної простатектомії; плевральна порожнина.
Спільне застосування хіміотерапії і ФДТ може підвищити результативність лікування. Це підтверджують роботи вітчизняних і зарубіжних авторів [http://www.magicray.ru/RU/lecture/L1/1.shtmll.].
Переваги ФДТ в лікуванні перерахованих пухлинних захворювань зазначених локалізацій сьогодні незаперечні. Дані про можливість використання фотодинамічної терапії в лікуванні злоякісних пухлин орбіти в доступній літературі відсутні. Це визначається відразу декількома моментами.
По-перше, важкою доступністю для проведення ФДТ як самостійного виду лікування без операції і розрізу; по-друге, замкнутістю і тіснотою простору, іменованого орбітою, де так тісно, що пухлина завбільшки з горошину викликає зміщення очного яблука з екзофтальм, величиною до 3 мм. Проведенню ФДТ при цьому перешкоджає обмеженість способу за глибиною проникнення в біологічні об'єкти - тканини. Випромінювання не проникає глибше 7 мм. Злоякісні пухлини орбіти, як правило, стеляться вздовж верхньої стінки, йдучи вглиб, до її вершини. А глибина орбіти, як відомо, коливається від 3 до 4,5 см. Ми припустили, що якщо ФДТ непридатна в якості самостійного способу лікування злоякісних пухлин орбіти, то вона може бути корисною в якості ад'ювантної місцевої терапії, що проводиться інтраопераційно в комбінації з орбітотомія з видаленням пухлини ad maximum і хіміотерапією. Ми спробували застосувати цей спосіб в лікуванні безнадійних пацієнтів. Як фотосенсибілізатора ми взяли вітчизняний препарат Фотосенс. Зазначений фотосенсибілізатор ввели в передопераційному періоді за 3 доби до проведення операції.
Таким чином, пропонований нами спосіб органозберігаючого лікування злоякісних пухлин орбіти, і як і спосіб, взятий нами за найближчий аналог, складається з комбінації, що включає орбітотомія з видаленням пухлини ad maximum, хіміотерапію та променеву терапію. Але, при цьому, наш спосіб має суттєві відмінності від аналога, які полягають в тому, як променевого методу ми пропонуємо фотодинамічної терапії. Для проведення ФДТ за 3 доби до операції вводять фотосенсибілізатор Фотосенс. Фотодинамічна терапія теоретично цілком може замінити дистанційну променеву терапію, при цьому вона повинна проводитися на операційному столі відразу після видалення пухлини ad maximum.
Перевагами пропонованого нами способу, на наш погляд, є вибірковість або адресна доставка променевого впливу в пухлинну тканину, що представляє депо фотосенсибілізатора. Це дозволяє звести до мінімуму постлучевая ускладнення дистанційної гамма-терапії у вигляді кератитів, атрофії зорового нерва, нейроретинопатии, кератопатії, катаракти і постлучевих иридоциклитов. До того ж резистентності будь-яких пухлин до ФДТ не відзначено. Наявність одночасно декількох механізмів пухлинної деструкції (запуск реакцій променевого апоптозу, фототромбоза, посттромботичного паравазального апоптозу, перекисного вибуху і т.д.) в арсеналі цього методу дозволяє сподіватися на успіх /http://www.magicray.m/RU/lecture/L1 /1.shtmll
Ми реалізували наш винахід на практиці і отримали підтвердження його правомочності і простоти в технічному виконанні.
Технічним результатом винаходу є повноцінна деструкція пухлини, розташованої в технічно доступної зоні - орбіті.
Технічний результат досягається завдяки комбінації трьох способів: орбітотоміі з видаленням пухлини ad maximum, фотодинамічної терапії з використанням певних доз фотосенсибілізатора Фотосенс і при рівномірному розподілі світлової енергії в порожнині орбіти після висічення пухлини і при обраному режимі лазерного впливу, а і хіміотерапії.
Мета орбітотоміі з видаленням пухлини ad maximum полягає в зменшенні обсягу / масиву злоякісної пухлини, що дозволяє підвищити ефективність подальшої фотодинамічної терапії із застосуванням фотосенсибілізатора Фотосенс. При цьому її ефективність підвищується завдяки більш рівномірному опроміненню залишків пухлини за рахунок використання циліндричного диффузорного світловода, зануреного у водне середовище, що є посередником між залишками пухлини і джерелом випромінювання. Наявність водного середовища сприяє більш рівномірному розподілу світлової енергії в порожнині орбіти. Хіміотерапія застосовується по одному з відомих класичних рекомендованих варіантів, наприклад, вінкристин + циклофосфан + актиноміцин Д або топотекан + циклофосфамід і / або топотекан + циклофосфамід + вінкристин або будь-яка інша схема, вибір якої визначається гістогенезом пухлини і її чутливістю до хіміопрепаратів [Baker KS, Anderson JR, Link MP, et al: Benefit of intensified therapy for patients with local or regional embryonal rhabdomyosarcoma: Results from the Intergroup Rhabdomyosarcoma Study IV. J Clin Oncol - 2000 - vol.18 - pp.2427-2434; Керівництво по офтальмоонкологіі. - Під керівництвом проф. А.Ф.Бровкіной. М .: Медицина, 2002 с.112].
При виборі доз Фотосенс ми орієнтувалися на той факт, що масив залишилася в орбіті пухлини не може бути великий, як при плевральних або внутрішньочеревно порожнинах, а отже, не повинен виходити за межі 1,0 мг / кг. Але разом з тим, вони не можуть бути нижче 0,1 мг / кг ваги хворого, оскільки інакше ми не зможемо досягти фотодеструкции пухлини через низьку концентрації препарату в пухлинному масиві. Депо препарату в пухлині буде недостатнім, коефіцієнт контрастності буде низьким і в процесі опромінення постраждають однаково і здорові навколишні тканини і тканини пухлини. Розвинеться фіброз орбіти.
При виборі доз світлової енергії ми базувалися на той факт, що біологічні ефекти фотодеструкции, що викликаються фотодинамічної терапії, розвиваються при значеннях світлової енергії не нижче 120 мВт / см 2, а при енергії вище 800 мВт / см 2 розвиваються побічні теплові ефекти, які ініціюють такі ускладнення , як уже згаданий фіброз орбіти.
СПОСІБ ЗДІЙСНЮЮТЬ наступним чином
На етапі планування операції за три доби до її проведення внутрішньовенно вводять фотосенсибілізатор Фотосенс в кількості, від 0,1 до 1 мг / кг ваги хворого в залежності від передбачуваного залишкового обсягу пухлини. Потім в зазначений термін (на третю добу), пацієнту проводять орбітотомія з видаленням пухлини ad maximum (видаляють основний масив пухлини без руйнування життєво важливих структур орбіти, що забезпечують життєдіяльність очі: м'язи, зоровий нерв).
В кінці операції відмивають ретробульбарні тканини від крові, заповнюють порожнину орбіти фізіологічним розчином, вводять циліндричний діффузорний світловод, за допомогою якого проводять опромінення лазерним випромінюванням з довжиною хвилі 670 нм, що знаходиться в максимумі спектра поглинання застосовуваного фотосенсибілізатора з сумарною щільністю потужності 120-800 мВт / см 2.
Операцію завершують після вилучення світловода, видалення фіз. розчину, ушиванием рани.
приклад
Пацієнтка 27 років. Д-з: третій рецидив рабдоміосаркоми правої орбіти. Екзофтальмометрія по Гертеля неможлива.
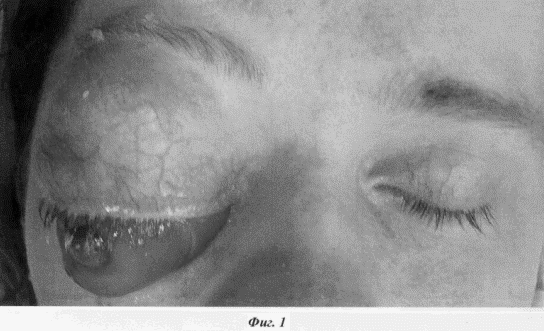
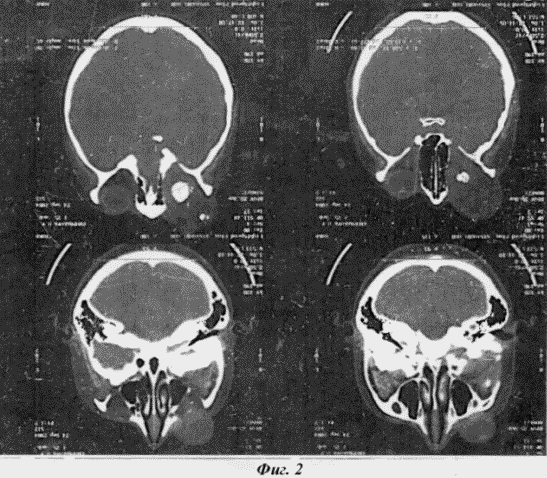
Око вивихнути з орбіти, практично «висить» на зоровому нерві (фіг.1). На представлених серійних знімках комп'ютерної томографії орбіти порожнину орбіти практично забиті пухлинними масами до самої вершини (фіг.2)
З анамнезу: 2 роки тому проведена орбітотомія, в післяопераційному періоді проведено стандартний курс хіміотерапії і променевої терапії на область орбіти з сумарною променевої дозою - 30 Гр. Рецидив настав через 1 рік після проведеного курсу. Знову отримала променеву терапію - 40 Гр і курс хіміотерапії. Перенесла лікування погано. Неодноразово наголошувала епізоди блювоти. Після курсу мав місце аллопеційний ефект з повним облисінням. Від запропонованої екзентерація категорично відмовляється. Проведено багаторазові бесіди в присутності чоловіка і матері пацієнтки. Наполягає на спробі органосохранное лікування. Попереджена про ризик можливих ускладнень, включаючи проростання в порожнину черепа і метастазування.
Введено фотосенсибілізатор Фотосенс з розрахунку 0,3 мг / кг ваги хворий, виходячи з факту передбачуваного обсягу залишкової пухлини не більше 5 см 3. На третю добу після загальноприйнятої реєстрації накопичення фотосенсибілізатора проведена орбітотомія з видаленням пухлини ad maximum, в ході якої видалений основний масив пухлини, рана відмита від крові. Порожнина заповнена фізіологічним розчином, потім введений циліндричний діффузорний світловод, за допомогою якого проведено опромінення на довжині хвилі 670 нм (максимум спектра поглинання застосовуваного фотосенсибілізатора Фотосенс) тканин пухлини з сумарною дозою 350 мВт / см 2. При виборі дози ми виходили з обсягу залишкової пухлини: пухлинна тканина залишалася практично тільки на стінках орбіти і у її вершини. Потім, по завершенні опромінення, рана була звільнена від фізіологічного розчину і світловода, ушита.
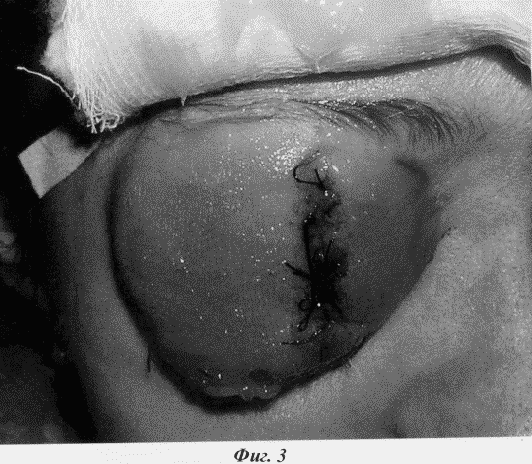
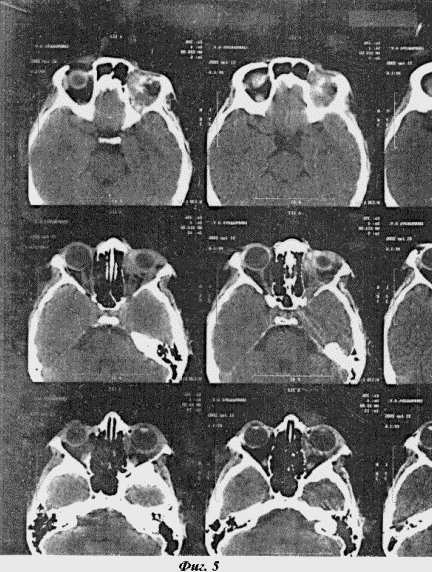
Гістологічні дослідження виявили ботріоідние тип рабдоміосаркоми, який є резистентним до променевої терапії. У післяопераційну періоді ми провели 3 курсу хіміотерапії. Використовували стандартну схему: вінкристин + циклофосфан + актиноміцин Д. Відразу після операції мав місце післяопераційний набряк тканин орбіти (фіг.3)
Через 2 тижні був відзначений позитивний ефект у вигляді зменшення набряку ретробульбарних і періорбітальний тканин, репозиції очного яблука в орбіту. 5 місяці по тому відзначається легкий енофтальм (западання очного яблука в орбіті), обумовлений втягнення очного яблука фіброзно-зміненими тканинами (фіг.4). Птоз до середини зіниці. Ознак пухлинного росту не відзначено.
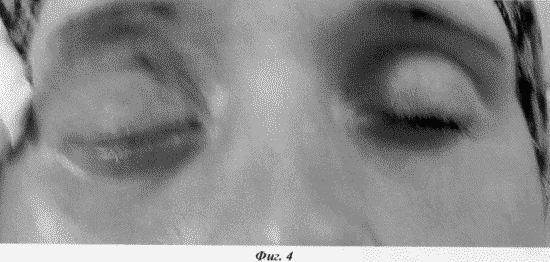
На контрольному КТ виявляється фіброз залишкової пухлинної тканини, що визначається по КТ-щільності (55 ОД Намсфелда), ознак продовженого росту або рецидиву пухлини немає.
На УЗД - зафіксовано появу кровотоку в магістральних судинах очі.
Гострота зору на хворому оці - 0,1.
Таким чином, проведене лікування дозволило зберегти пацієнтці очей як орган, вберегти її від проростання пухлини в порожнину черепа і зберегти їй життя, а й істотно підвищити якість її життя. Запропонований спосіб може бути альтернативою екзентерація і комбінації орбітотоміі + променевої терапії (дистанційної гамма-терапії) + хіміотерапії.
Перевагами пропонованого нами способу є прискорення процесу реабілітації. Він дозволяє уникнути такої факт, як променева резистентність і весь широкий ряд постлучевих ускладнень у вигляді иридоциклитов, катаракти, нейроретинопатии, атрофії зорового нерва, постлучевих дерматитів, кератитів і кератопатію, склеромаляцій і субатрофія очного яблука та ін.
ФОРМУЛА ВИНАХОДУ
Спосіб комбінованого органозберігаючого лікування злоякісних пухлин орбіти, що включає орбітотомія з видаленням пухлини ad maximum, интраоперационную променеву терапію і хіміотерапію, що відрізняється тим, що в якості променевої терапії використовують фотодинамічної терапії, для чого за 3 доби до операції внутрішньовенно вводять Фотосенс в дозі 0,1 мг / г ваги, а безпосередньо після видалення пухлини і відмивання операційної рани від крові заповнюють порожнину фізіологічним розчином, вводять в неї циліндричний діффузорний світловод і проводять лазерне вплив з довжиною хвилі 670 нм і щільністю потужності від 120 до 800 мВт / см 2, після чого видаляють фізіологічний розчин, витягають світловод і вшивають рану.
Версія для друку
Дата публікації 06.01.2007гг




Коментарі
Коментуючи, пам'ятайте про те, що зміст і тон Вашого повідомлення можуть зачіпати почуття реальних людей, проявляйте повагу та толерантність до своїх співрозмовників навіть у тому випадку, якщо Ви не поділяєте їхню думку, Ваша поведінка за умов свободи висловлювань та анонімності, наданих інтернетом, змінює не тільки віртуальний, але й реальний світ. Всі коменти приховані з індексу, спам контролюється.